Ученым удалось вырастить в эмбрионе свиньи аналог человеческой почки
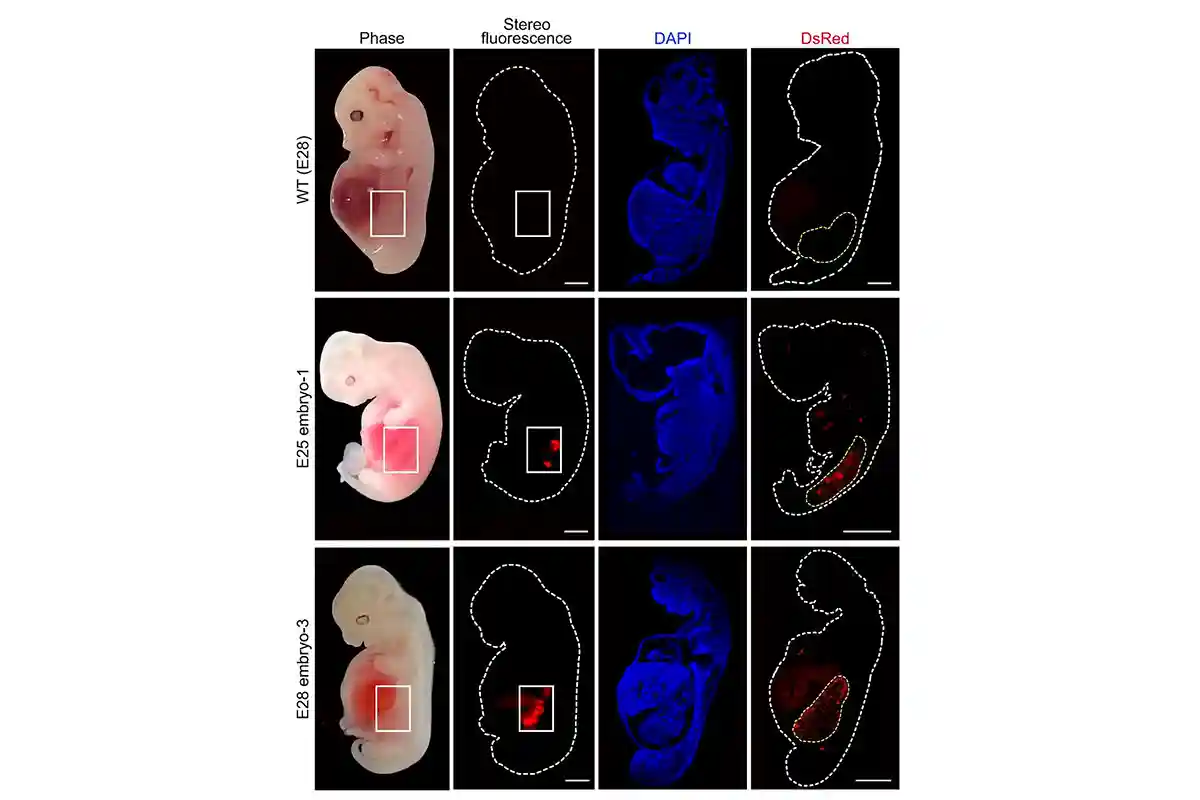
Ученым удалось вырастить в эмбрионе свиньи аналог человеческой почки
Ученым удалось вырастить в эмбрионе свиньи почечную ткань с преобладанием человеческих клеток. Для этого они выключили в эмбрионах два гена, важных для развития почек. Затем в этом месте органа может вырасти почечная ткань из человеческих стволовых клеток. Выращенные таким образом органы впоследствии могут стать донорскими. Группа под руководством Лянсюэ Лая (Liangxue Lai) из Института биомедицины и здоровья в Гуанчжоу (Китай) представляет свой подход в научном журнале «Cell Stem Cell».
«Органы крысы были получены в организме мышей, а органы мыши – в организме крыс, но предыдущие попытки вырастить человеческие органы в организме свиней не увенчались успехом», – поясняет Лай. Проблема та же, что и при донорстве органов, когда донор и реципиент плохо подходят друг другу. Тогда орган отторгается организмом реципиента, поскольку иммунная система распознает его как чужеродную ткань и начинает защитные меры. Кроме того, клетки свиньи в эмбрионе способны удерживать свои позиции лучше, чем клетки человека, и оба типа клеток имеют различные потребности для процветания.
Используя генные ножницы Crispr/Cas, исследователи удалили из одноклеточного эмбриона свиньи гены SIX1 и SALL1, необходимые для развития почек. В результате у эмбриона не развились свиные почки, образовав вакансию или нишу. В эмбрион были введены человеческие плюрипотентные стволовые клетки, полученные из пуповинной крови, которые могут давать начало всем видам человеческих клеток. Они смогли развиться в ткань почки в созданной нише практически без конкуренции.
Стволовые клетки человека были предварительно специально подготовлены. С одной стороны, генетическое вмешательство привело к повышенной активации генов MYCN и BCL2. Оба гена обеспечивают выживаемость клеток, в случае BCL2 – предотвращая запрограммированную гибель клеток (апоптоз). Во-вторых, ученые поместили стволовые клетки в недавно разработанную культуральную среду (4CL), которая заставляет стволовые клетки переходить на более ранние стадии развития, в результате чего они становятся похожими на ранние эмбриональные клетки человека.Эмбрионы свиней имплантировали свиноматкам, где они развивались до 25–28-го дня. В некоторых эмбрионах почка, созданная в основном из человеческих клеток, развивалась нормально по сравнению с необработанными свиными эмбрионами. Однако процедура все еще требует усовершенствования: «Общая доля дегенерирующих свиных эмбрионов высока, и необходимо оценить, связано ли это отчасти с химеризмом или другими аспектами процедуры инъекции», – пишут авторы исследования.Более того, даже хорошо выращенные почки все еще содержат более трети клеток свиней, что может привести к защитным реакциям в организме человека при трансплантации органов. «Поскольку органы состоят не только из одной клеточной линии, нам, вероятно, придется проводить гораздо более сложные манипуляции со свиньями, чтобы получить орган, в котором все клетки будут от человека», – говорит соавтор исследования Мигель Эстебан из Института биомедицины и здоровья в Гуанчжоу.
Пуповинная кровь как основа стволовых клеток человека
Специалист по медицинской этике Вольфрам Хенн из Немецкого совета по этике в своей оценке исследования положительно отмечает, что в качестве основы для стволовых клеток человека была использована пуповинная кровь. Это позволяет избежать использования человеческих эмбрионов. Кроме того, данная процедура открывает перспективы того, что в будущем собственные стволовые клетки крови пациента, зависящие от донорского органа, могут быть использованы в качестве основы для выращивания органа. Поскольку в этом случае клетки будут получены от самого пациента, реакции отторжения, как правило, не должно быть. В целом он считает подход исследователей разумным и ответственным.
Хенн также считает процедуру этически оправданной с точки зрения защиты животных: «Мы разводим животных, чтобы их есть, поэтому нет ничего предосудительного в том, чтобы разводить животных для спасения человеческих жизней». Хенн считает важным, прежде всего, модернизацию немецкого законодательства, поскольку Закону о защите эмбрионов уже более 30 лет. Многие из процедур, используемых сегодня, не существовали в то время, поэтому правовая база для исследований, подобных описанным в работе, должна быть переписана, требует специалист по медицинской этике.
Читайте также:
- Ученые обнаружили динозавра с самой длинной шеей на сегодняшний день
- Ученые: изменения климата приводят к прогрессу
- Ученые спрогнозировали вымирание человечества к 2100 году