Marea Britanie autorizează prima terapie cu foarfecă genetică
În Marea Britanie, un medicament bazat pe tehnologia Crispr, care utilizează o foarfecă genetică, a fost autorizat pentru prima dată în lume. Acest lucru a fost anunțat de către Agenția de Reglementare a Medicamentelor și a Produselor de Sănătate (MHRA).
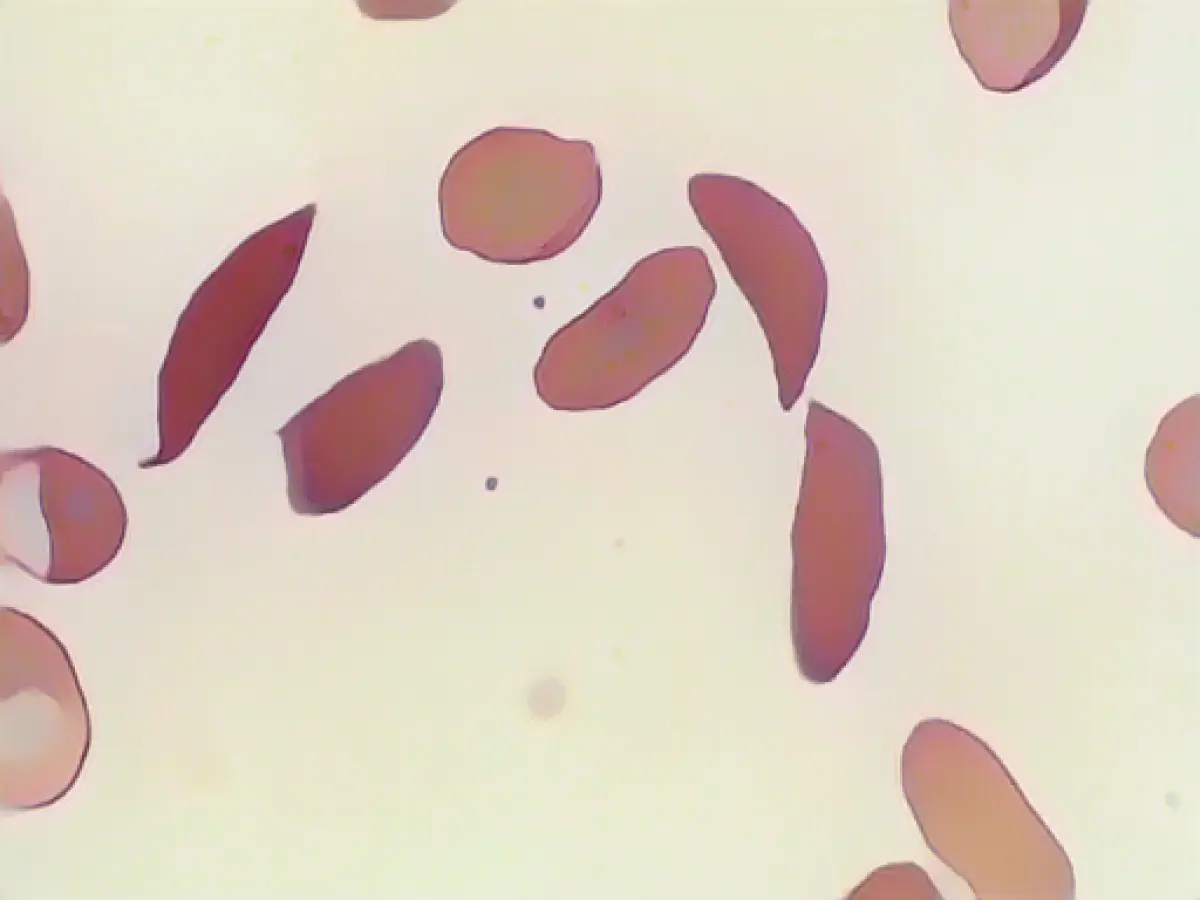
Medicamentul, denumit "Casgevy", a fost aprobat pentru tratamentul bolii celulelor secerătoare și al beta talasemiei la pacienții cu vârsta de peste 12 ani. Ambele afecțiuni genetice ale sângelui sunt cauzate de erori în gena hemoglobinei. Acesta este un complex proteic care conține fier și care se găsește în celulele roșii din sânge și este folosit pentru a transporta oxigenul.
Sunt necesare șederi lungi în spital
Așa-numita foarfecă genetică Crispr/Cas poate fi folosită pentru a ținti gene individuale. Dezvoltatorii metodei, Emmanuelle Charpentier și Jennifer A. Doudna, au primit Premiul Nobel pentru aceasta în 2020. "Casgevy" este utilizată pentru a modifica genele defecte din celulele stem din măduva osoasă a pacienților, astfel încât acestea să poată produce hemoglobină funcțională, potrivit unui comunicat al MHRA. Pentru a face acest lucru, celulele stem sunt prelevate din măduva osoasă, prelucrate în laborator și apoi reintroduse în pacient. Terapia necesită ca pacientul să fie spitalizat timp de câteva săptămâni. Cu toate acestea, rezultatul are potențialul de a avea un efect pe toată durata vieții, continuă raportul.
Atât boala celulelor secerătoare, cât și beta talasemia sunt afecțiuni dureroase, care durează toată viața și care, în unele cazuri, pot fi fatale, a declarat Julian Beach, director executiv interimar al diviziei de calitate și acces la asistență medicală din cadrul MHRA. El a adăugat: "Până acum, un transplant de măduvă osoasă - care trebuie să provină de la un donator bine compatibil și care prezintă riscul de respingere - a fost singura opțiune de tratament permanent".
Boala celulelor secerătoare poate duce la crize severe de durere, infecții grave și care pun viața în pericol și anemie, cunoscută și sub numele de anemie, o lipsă de oxigen în sânge. Pacienții cu beta-talasemie suferă, de asemenea, de anemie și au adesea nevoie de transfuzii de sânge la fiecare trei până la cinci săptămâni.
Fără atacuri de durere severe
Dintre cei 28 de pacienți cu anemie falciformă care au fost tratați cu acest medicament în cadrul unui studiu clinic, 97% au fost, conform rapoartelor, scutiți de crize de durere severă timp de cel puțin un an. În cadrul studiului clinic cu pacienți cu beta-talasemie dependenți de transfuzii de sânge, 93 la sută (39 din 42 de pacienți) nu au avut nevoie de o transfuzie de globule roșii timp de cel puțin douăsprezece luni. La ceilalți trei pacienți, a fost posibilă o reducere de cel puțin 70 la sută a transfuziilor de sânge.
Medicamentul este produs în cadrul unei colaborări între companiile Vertex și CRISPR Therapeutics, care au sediile în SUA și Elveția. Potrivit unui comunicat al celor două companii, în prezent, aproximativ 2000 de persoane din Marea Britanie sunt susceptibile de a fi eligibile pentru tratamentul cu "Casgevy". Directorul general al Vertex, Reshma Kewalramani, a vorbit despre o "zi istorică în știință și medicină". El speră că aceasta este doar prima dintre numeroasele aplicații ale metodei de care ar putea beneficia persoanele cu boli grave, a declarat directorul general al CRISPR Therapeutics, Samarth Kulkarni, potrivit comunicatului de presă.
Sursawww.dpa.com